Категории
- Болезнь Альцгеймера
- Болезнь Меньера
- Болезнь Паркинсона
- Витамины
- Иммунная система
- Иммунодепрессанты
- Мама и ребенок
- Противоаллергические средства
- Противогрибковые препараты
- Противосудорожные препараты
- Противоэпилептические средства
- Сахарный диабет
- Гормоны
- Дерматология
- Дыхательная система
- Кроветворение и кровь
- Мочеполовая система и половые гормоны
- Нервная система
- Онкология
- Опорно-двигательный аппарат
- Пищеварительный тракт и обмен веществ
- Препараты для лечения заболеваний органов чувств
- Противомикробные препараты для системного применения
- Противопаразитарные препараты, инсектициды и репелленты
- Сердечно-сосудистая система
- Прочее
100% Гарантия платежных обязательств
Заказанный препарат будет доставлен Вам в указанный срок. В случае отказа будет произведен возврат средств. Мы ценим каждого клиента и понимаем его потребности.
СоглашениеВам также могут подойти
Конфиденциальность
Любая информация о совершенных покупках клиента, его личных данных не разглашается и не передается. Мы соблюдаем максимум приватности в своей работе.
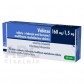
СоглашениеЛамиктал (Lamictal) 5 мг, 60 таблеток
Код товара: Ламиктал (Lamictal) 5 мг, 60 таблеток
Доступность: На складе
Доставляем препараты в страны:
Таджикистан Армения Азербайджан Грузия
Узбекистан Киргизия (Кыргызстан)
Похожие товары
Ламиктал (Lamictal)
Действующее вещество
Ламотриджин* (Lamotrigine*)
ATX N03AX09 Ламотриджин
Фармакологическая группа
Противоэпилептические средства
Характеристика
Порошок от белого до бледно-кремового цвета, очень слабо растворим в воде (0,17 мг/мл при 25 °C) и слабо растворим в 0,1 М растворе соляной кислоты (4,1 мг/мл при 25 °C). Молекулярная масса 256,09 Да.
Фармакология
Противоэпилептическое ЛС класса фенилтриазинов.
Механизм действия
Точный механизм противосудорожного действия ламотриджина неизвестен. В моделях на животных, разработанных для определения противосудорожной активности, ламотриджин демонстрировал эффективность в предотвращении развития судорожных припадков в тестах максимального электрошока и с пентилентетразолом, а также предотвращал развитие судорог в тестах, в которых провокаторами судорожных припадков выступают зрительные раздражители или электрический ток. Ламотриджин также проявлял ингибирующие свойства в киндлинг-модели у крыс как в процессе стимуляции, так и в состоянии установившегося киндлинга. Однако применимость этих моделей для эпилепсии у человека неизвестна.
Один из предполагаемых механизмов действия ламотриджина, значимость которого для человека еще предстоит установить, связан с воздействием на натриевые каналы. Фармакологические исследования in vitro показывают, что ламотриджин ингибирует потенциалзависимые натриевые каналы, тем самым стабилизируя мембраны нейронов и, следовательно, модулируя высвобождение пресинаптических медиаторов возбуждающих аминокислот (например, глутамат и аспартат).
Влияние ламотриджина на опосредованную N-метил-D-аспартат-рецептором активность
Ламотриджин не ингибировал N-метил-D-аспартат (NMDA)-индуцированную деполяризацию в срезах коры головного мозга у крыс или NMDA-индуцированное образование цГМФ в незрелом мозжечке крысы, а также не вытеснял соединения, которые являются конкурентными или неконкурентными лигандами глутаматных рецепторов (CNQX, CGS, TCHP). IC50 ламотриджина в отношении NMDA-индуцированных ионных токов (в присутствии 3 мкмолей глицина) в культивируемых нейронах гиппокампа превышала 100 мкмоль.
Механизмы терапевтического действия ламотриджина при биполярном расстройстве не установлены.
Фармакодинамика
Метаболизм фолатов
In vitro ламотриджин ингибировал дигидрофолатредуктазу — фермент, катализирующий восстановление дигидрофолата до тетрагидрофолата. Ингибирование этого фермента может препятствовать биосинтезу нуклеиновых кислот и белков. При пероральном введении суточных доз ламотриджина беременным крысам в период органогенеза концентрация фолатов в плаценте, организме матери и плода снижалась. Значительно сниженные концентрации фолатов связаны с тератогенезом (см. «Применение при беременности и кормлении грудью»). Концентрация фолатов была также снижена у самцов крыс, получавших многократные пероральные дозы ламотриджина. Сниженные концентрации частично возвращались к норме при добавлении фолиевой кислоты.
Кумуляция в почках
Ламотриджин накапливался в почках самцов крыс, вызывая хронический прогрессирующий нефроз, некроз и минерализацию. Эти результаты обусловлены наличием α2-микроглобулина, белка специфичного для вида и пола, который не был обнаружен у других животных или человека.
Связывание с меланином
Ламотриджин связывается с меланинсодержащими тканями, например в глазах и пигментированной коже. Он был обнаружен в увеальном тракте у грызунов через 52 нед после введения однократной дозы.
ССС
У собак ламотриджин интенсивно метаболизируется до 2-N-метилового метаболита. Этот метаболит вызывает дозозависимое удлинение интервала PR, расширение комплекса QRS, а при более высоких дозах — полную блокаду AV-проводимости. Подобные сердечно-сосудистые эффекты у человека не ожидаются, поскольку в моче человека были обнаружены лишь следовые количества 2-N-метилового метаболита (<0,6% от дозы ламотриджина). Однако можно предположить, что концентрация этого метаболита в плазме крови может быть повышена у пациентов с пониженной способностью к глюкуронизации ламотриджина (например, у пациентов с заболеваниями печени, у пациентов, принимающих сопутствующие ЛС, ингибирующие глюкуронизацию).
Фармакокинетика
Фармакокинетика ламотриджина изучалась у пациентов с эпилепсией, здоровых молодых и пожилых добровольцев и добровольцев с ХПН. Фармакокинетические параметры ламотриджина для взрослых пациентов, детей и здоровых добровольцев приведены в таблицах 1 и 2 (см. Особые группы пациентов. Дети).
Таблица 1
Средние фармакокинетические параметры1 у здоровых добровольцев и взрослых пациентов с эпилепсией
1 Большинство средних значений параметров, определенных в каждом исследовании, имели коэффициенты вариации от 20 до 40% для T1/2 и Cl/F и от 30 до 70% — для Tmax. Общие средние значения были рассчитаны на основе средних значений в отдельных исследованиях, которые были оценены на основе количества добровольцев/пациентов в каждом исследовании. Цифры в скобках под каждым средним значением параметра отражают диапазон значений отдельных добровольцев/пациентов в рамках исследований.
2 Cl/F — средний кажущийся клиренс из плазмы крови.
3 Было показано, что карбамазепин, фенитоин, фенобарбитал и примидон увеличивают кажущийся клиренс ламотриджина. Эстрогенсодержащие пероральные контрацептивы и другие ЛС, такие как рифампицин и ингибиторы протеазы лопинавир/ритонавир и атазанавир/ритонавир, которые индуцируют глюкуронизацию ламотриджина, также увеличивают кажущийся клиренс ламотриджина (см. «Взаимодействие»).
Абсорбция
Ламотриджин быстро и полностью всасывается после перорального приема с незначительным метаболизмом первого прохождения через печень (абсолютная биодоступность составляет 98%). Прием пищи не влияет на биодоступность ламотриджина. Tmax в плазме крови после приема ламотриджина составляет 1,4–4,8 ч.
Установлено, что скорость и степень всасывания ламотриджина не зависят от его лекарственной формы и способа применения.
У здоровых добровольцев, не получавших другие ЛС и принимавших однократные дозы ламотриджина, концентрация ламотриджина в плазме крови повышалась прямо пропорционально дозе в диапазоне от 50 до 400 мг. В двух небольших исследованиях (n=7 и 8) с участием пациентов с эпилепсией, принимавших другие противоэпилептические ЛС, также наблюдалась линейная зависимость между дозой и концентрацией ламотриджина в плазме крови в равновесном состоянии после приема в дозах от 50 до 350 мг 2 раза в день.
Распределение
Значение среднего кажущегося Vd ламотриджина после перорального приема варьировало от 0,9 до 1,3 л/кг, не зависело от дозы и оставалось неизменным после однократного и многократного приема как у пациентов с эпилепсией, так и у здоровых добровольцев.
Данные исследований in vitro показывают, что ламотриджин примерно на 55% связывается с белками плазмы крови человека при его концентрации в плазме крови от 1 до 10 мкг/мл (концентрация 10 мкг/мл в 4–6 раз превышает концентрацию в плазме крови, наблюдавшуюся в контролируемых исследованиях эффективности). Поскольку ламотриджин слабо связывается с белками плазмы крови, клинически значимое взаимодействие с другими ЛС через конкуренцию за места связывания с белками маловероятно. Связывание ламотриджина с белками плазмы крови не изменялось в присутствии терапевтических концентраций фенитоина, фенобарбитала или вальпроата. Ламотриджин не вытеснял другие противоэпилептические ЛС (карбамазепин, фенитоин, фенобарбитал) из мест связывания с белками плазмы крови.
Метаболизм
Ламотриджин метаболизируется преимущественно путем конъюгации с глюкуроновой кислотой, основным метаболитом является неактивный конъюгат 2-N-глюкуронида. После перорального приема 240 мг 14C-меченного ламотриджина (15 мкКи) 6 здоровыми добровольцами 94% выводилось с мочой и 2% — с калом. Радиоактивность в моче определялась в виде неизмененного ламотриджина (10%), 2-N-глюкуронида (76%), 5-N-глюкуронида (10%), 2-N-метилового метаболита (0,14%) и других неидентифицированных второстепенных метаболитов (4%).
Влияние ламотриджина на индукцию отдельных семейств изоферментов оксидазы со смешанной функцией не подвергалось систематической оценке.
После многократного приема ламотриджина (150 мг 2 раза в день) здоровыми добровольцами, не принимавшими другие ЛС, ламотриджин индуцировал собственный метаболизм, что приводило к снижению T1/2 на 25% и увеличению Cl/F на 37% в равновесном состоянии по сравнению со значениями, полученными у тех же добровольцев после однократного приема. Данные, полученные из других источников, свидетельствуют о том, что самоиндукция ламотриджина может не происходить, если ламотриджин назначается в качестве дополнительной терапии пациентам, получающим ферментиндуцирующие ЛС, такие как карбамазепин, фенитоин, фенобарбитал, примидон, или другие ЛС, такие как рифампицин и ингибиторы протеазы лопинавир/ритонавир и атазанавир/ритонавир, которые индуцируют глюкуронизацию ламотриджина (см. «Взаимодействие»).
Элиминация
T1/2 и кажущийся клиренс ламотриджина после перорального приема взрослыми пациентами с эпилепсией и здоровыми добровольцами обобщены в таблице 1 и зависят от применения сопутствующих противоэпилептических ЛС.
Особые группы пациентов
Почечная недостаточность.12 добровольцев с ХПН (средний Cl креатинина 13 мл/мин, диапазон 6–23 мл/мин) и еще 6 пациентов, находящихся на гемодиализе, получили однократную дозу ламотриджина 100 мг. Средний T1/2 из плазмы крови, определенный в ходе исследования, составил 42,9 ч (ХПН), 13 ч (во время гемодиализа) и 57,4 ч (между сеансами гемодиализа) по сравнению с 26,2 ч у здоровых добровольцев. В среднем, приблизительно 20% (диапазон 5,6–35,1) от количества ламотриджина, присутствующего в организме, выводилось при гемодиализе в течение 4-часового сеанса.
Печеночная недостаточность. Фармакокинетику ламотриджина после однократного приема в дозе 100 мг оценивали у 24 пациентов с печеночной недостаточностью легкой, средней и тяжелой степени тяжести (тяжелая степень без асцита (n=2) или с асцитом (n=5) по классификации Чайлд-Пью) и сравнивали с данными, полученными у 12 пациентов без печеночной недостаточности. Значение Cl/F ламотриджина у пациентов с печеночной недостаточностью легкой (n=12), средней (n=5), тяжелой без асцита (n=2) и тяжелой с асцитом (n=5) степени тяжести составляло (0,3±0,09), (0,24±0,1), (0,21±0,04) и (0,15±0,09) мл/мин/кг соответственно, по сравнению с (0,37±0,1) мл/мин/кг у здоровых пациентов. Средний T1/2 ламотриджина у пациентов с печеночной недостаточностью легкой, средней, тяжелой без асцита и тяжелой с асцитом степени тяжести составлял (46±20), (72±44), (67±11) и (100±48) ч соответственно, по сравнению с (33±7) ч у здоровых пациентов.
Дети. Фармакокинетика ламотриджина после приема однократной дозы 2 мг/кг оценивалась в двух исследованиях у детей (n=29 для пациентов от 10 мес до 5,9 лет и n=26 для пациентов 5–11 лет). 43 пациента получали сопутствующую терапию ламотриджином и другими противоэпилептическими ЛС, а 12 пациентов — ламотриджин в качестве монотерапии. Фармакокинетические параметры ламотриджина для педиатрических пациентов обобщены в таблице 2.
Популяционный фармакокинетический анализ с участием пациентов от 2 до 18 лет показал, что на клиренс ламотриджина в основном влияет общая масса тела и сопутствующая терапия противоэпилептическими ЛС. Клиренс ламотриджина при пероральном приеме (теоретический клиренс ламотриджина) с учетом массы тела был выше у детей, чем у взрослых. Нормализованный по массе тела клиренс ламотриджина был выше у пациентов с массой тела менее 30 кг по сравнению с пациентами с массой тела более 30 кг. Соответственно, пациентам с массой тела менее 30 кг может потребоваться увеличение поддерживающих доз на 50% в зависимости от клинического ответа, по сравнению с пациентами с массой тела более 30 кг, получающими те же противоэпилептические ЛС. Также показано, что с учетом массы тела клиренс ламотриджина существенно не зависит от возраста. Таким образом, детям следует назначать одинаковые дозы с поправкой на массу тела независимо от возраста. Установлено, что сопутствующие противоэпилептические ЛС, которые влияют на клиренс ламотриджина у взрослых, оказывают аналогичное влияние и у детей.
Таблица 2
Средние фармакокинетические параметры ламотриджина у детей с эпилепсией1
1 Было показано, что карбамазепин, фенитоин, фенобарбитал и примидон увеличивают кажущийся клиренс ламотриджина. Эстрогенсодержащие пероральные контрацептивы, рифампицин и ингибиторы протеазы лопинавир + ритонавир и атазанавир + ритонавир также увеличивают кажущийся клиренс ламотриджина (см. «Взаимодействие»).
2 В расчет среднего значения Tmax были включены два пациента.
3 Параметр не оценивался.
Пожилой возраст. Фармакокинетика ламотриджина после приема однократной дозы 150 мг оценивалась у 12 добровольцев пожилого возраста от 65 до 76 лет (средний Cl креатинина 61 мл/мин, диапазон 33–108 мл/мин). Средний T1/2 ламотриджина у этих пациентов составил 31,2 ч (диапазон 24,5–43,4 ч), а средний клиренс — 0,40 мл/мин/кг (диапазон 0,26–0,48 мл/мин/кг).
Пол. Половая принадлежность не оказывает влияния на клиренс ламотриджина. Однако при повышении дозы ламотриджина в одном клиническом исследовании у пациентов с эпилепсией, принимавших стабильную дозу вальпроата (n=77), средняя Cmin ламотриджина без учета массы тела была на 24–45% выше (0,3–1,7 мкг/мл) у женщин, чем у мужчин.
Раса. Кажущийся общий клиренс ламотриджина был на 25% ниже у представителей неевропеоидной расы по сравнению с таковым у европеоидной расы.
Канцерогенность, мутагенность, влияние на фертильность
Никаких признаков канцерогенности не наблюдалось у мышей или крыс после перорального введения ламотриджина в течение 2 лет в дозах до 30 и от 10 до 15 мг/кг/сут соответственно. Самая высокая испытанная доза была ниже, чем доза 400 мг/сут ламотриджина для человека в расчете на площадь поверхности тела.
Ламотриджин показал отрицательный результат в анализах мутации генов in vitro (тест Эймса и тимидинкиназы в клетках мышиной лимфомы) и в анализах кластогенности (лимфоциты человека in vitro и костный мозг крысы in vivo).
У крыс, получавших пероральные дозы ламотриджина до 20 мг/кг/сут, не было обнаружено признаков нарушения фертильности. Самая высокая испытанная доза была ниже, чем доза 400 мг/сут ламотриджина для человека в пересчете на площадь поверхности тела.
Клинические исследования
Эпилепсия
Монотерапия ламотриджином у взрослых пациентов с парциальными припадками, уже получающих терапию карбамазепином, фенитоином, фенобарбиталом или примидоном в качестве единственного противоэпилептического ЛС. Эффективность монотерапии ламотриджином была установлена в ходе многоцентрового двойного слепого клинического исследования с участием 156 взрослых амбулаторных пациентов с парциальными припадками. Пациенты испытали не менее 4 простых парциальных, сложных парциальных и/или вторично-генерализованных припадка в течение каждого из 2 последовательных 4-недельных периодов, когда они получали монотерапию карбамазепином или фенитоином в течение этапа первичного обследования. Ламотриджин (целевая доза 500 мг/сут) или вальпроат (1000 мг/сут) добавляли к монотерапии карбамазепином или фенитоином в течение 4-недельного периода. Затем пациентов переводили на монотерапию ламотриджином или вальпроатом в течение следующих 4 нед, после чего продолжали монотерапию в течение дополнительного 12-недельного периода.
Конечной точкой исследования являлось завершение всех недель экспериментального лечения или достижение критерия выхода из исследования. Критериями выхода относительно этапа первичного обследования являлись:
- удвоение среднемесячного количества припадков;
- удвоение наибольшей частоты последовательных 2-дневных припадков;
- возникновение нового типа припадков (определяется как припадок, который не возникал в течение 8-недельного этапа включения), более тяжелого, чем припадки, случавшиеся в ходе лечения в рамках исследования;
- клинически значимое удлинение генерализованных тонико-клонических припадков.
Первичной переменной эффективности была доля пациентов в каждой группе лечения, которые соответствовали критериям выхода из исследования.
Процент пациентов, отвечавших критериям выхода, составил 42% (32 из 76) в группе, принимавшей ламотриджин, и 69% (55 из 80) — в группе получавших вальпроат. Разница в доле пациентов, отвечающих критериям выхода, была статистически значимой (p=0,0012) в пользу ламотриджина. Различий в эффективности в зависимости от возраста, пола или расы не выявлено.
Пациенты в контрольной группе намеренно получали относительно низкую дозу вальпроата, таким образом, единственной целью данного исследования была демонстрация эффективности и безопасности монотерапии ламотриджином, что не может быть истолковано как подразумевающее превосходство приема ламотриджина над адекватной дозой вальпроата.
Дополнительная терапия ламотриджином у взрослых пациентов с парциальными припадками. Эффективность применения ламотриджина в дополнение к другим противоэпилептическим ЛС была первоначально установлена в ходе 3 основных многоцентровых плацебо-контролируемых двойных слепых клинических исследований с участием 355 взрослых пациентов с рефрактерными парциальными припадками. Пациенты имели в анамнезе не менее 4 парциальных припадков в месяц, несмотря на прием одного или более противоэпилептических ЛС в терапевтических концентрациях, и в 2 исследованиях они наблюдались при установленной схеме приема противоэпилептических ЛС в течение этапа первичного обследования, продолжительность которого варьировала от 8 до 12 нед. В 3-м исследовании пациенты в течение проспективного этапа не наблюдались. У пациентов, продолжавших испытывать не менее 4 припадков в месяц в течение этапа первичного обследования, к существующей терапии добавляли прием ламотриджина или плацебо. Во всех 3 исследованиях основным показателем эффективности считалось изменение частоты возникновения припадков по сравнению с таковой в течение этапа первичного обследования. Приведенные ниже результаты относятся ко всем парциальным припадкам у всех назначенных к лечению пациентов, принявших хотя бы 1 дозу ЛС в каждом исследовании, если не указано иное. Медиана частоты возникновения припадков в течение этапа первичного обследования составляла 3 в неделю, а средняя частота возникновения припадков — 6,6 в неделю для всех пациентов, участвовавших в исследованиях эффективности.
Первое исследование (n=216) представляло собой двойное слепое плацебо-контролируемое исследование с параллельными группами, состоящее из 24-недельного периода лечения. Пациенты не могли принимать более 2 различных противосудорожных ЛС, прием вальпроата не допускался. Пациенты были рандомизированы для получения плацебо и целевой дозы ламотриджина 300 или 500 мг/сут. Медиана снижения частоты возникновения всех парциальных припадков по сравнению с периодом первичного обследования составила 8% у пациентов, получавших плацебо, 20% у пациентов, получавших ламотриджин в дозе 300 мг/сут, и 36% у пациентов, получавших ламотриджин в дозе 500 мг/сут. Снижение частоты возникновения припадков было статистически значимым в группе ламотриджина 500 мг/сут по сравнению с группой плацебо, но не в группе ламотриджина 300 мг/сут.
Второе исследование (n=98) представляло собой двойное слепое плацебо-контролируемое рандомизированное перекрестное исследование, состоящее из двух 14-недельных периодов лечения (последние 2 нед из которых приходились на период снижения дозы), разделенных 4-недельным периодом вымывания. Пациенты не могли принимать более 2 различных противосудорожных ЛС, прием вальпроата не допускался. Целевая доза ламотриджина составляла 400 мг/сут. Анализ первых 12 нед обоих периодов лечения показал снижение медианы изменения частоты возникновения припадков на 25% при приеме ламотриджина по сравнению с плацебо (p<0,001).
Третье исследование (n=41) представляло собой двойное слепое плацебо-контролируемое перекрестное исследование, состоящее из двух 12-недельных периодов лечения, разделенных 4-недельным периодом вымывания. Пациенты не могли принимать более 2 различных противосудорожных ЛС. 13 пациентов принимали сопутствующий вальпроат, эти пациенты получали ламотриджин в дозе 150 мг/сут. У 28 пациентов целевая доза ламотриджина составляла 300 мг/сут. Медиана изменения частоты возникновения припадков снизилась на 26% при приеме ламотриджина по сравнению с плацебо (p<0,01).
Различий в эффективности в зависимости от возраста, пола или расы, измеряемых изменением частоты возникновения припадков, не выявлено.
Дополнительная терапия ламотриджином у детей с парциальными припадками. Эффективность применения ламотриджина в качестве дополнительной терапии у детей с парциальными припадками была установлена в многоцентровом двойном слепом плацебо-контролируемом исследовании с участием 199 пациентов от 2 до 16 лет (98 из них принимали ламотриджин, 101 — плацебо). После 8-недельного этапа первичного обследования пациенты были рандомизированы на 18-недельное получение ламотриджина или плацебо дополнительно к текущей схеме, включавшей применение до 2 противоэпилептических ЛС. Пациенты получали дозу в зависимости от массы тела и приема вальпроата. Целевые дозы составляли примерно 5 мг/кг/сут для пациентов, принимающих вальпроат (максимальная доза 250 мг/сут), и 15 мг/кг/сут для пациентов, не принимающих вальпроат (максимальная доза 750 мг/сут). Первичной конечной точкой эффективности являлось процентное изменение количества всех парциальных припадков по сравнению с периодом первичного обследования. Для всех включенных в исследование пациентов, принявших хотя бы 1 дозу ЛС, медиана снижения количества всех парциальных припадков составила 36% у пациентов, принимавших ламотриджин, и 7% у пациентов, принимавших плацебо, что является статистически значимой разницей (p<0,01).
Дополнительная терапия ламотриджином у детей и взрослых пациентов с синдромом Леннокса-Гасто. Эффективность применения ламотриджина в качестве дополнительной терапии у пациентов с синдромом Леннокса-Гасто была установлена в многоцентровом двойном слепом плацебо-контролируемом исследовании с участием 169 пациентов от 3 до 25 лет (79 из них принимали ламотриджин, 90 — плацебо). После 4-недельной слепой фазы с приемом плацебо пациенты были рандомизированы на 16-недельное лечение ламотриджином или плацебо дополнительно к текущей схеме, включавшей применение до 3 противоэпилептических ЛС. Пациенты получали фиксированные дозы в зависимости от массы тела и приема вальпроата. Целевые дозы составляли примерно 5 мг/кг/сут для пациентов, принимающих вальпроат (максимальная доза 200 мг/сут), и 15 мг/кг/сут для пациентов, не принимающих вальпроат (максимальная доза 400 мг/сут). Первичной конечной точкой эффективности являлось процентное изменение количества больших моторных припадков (атонические, тонические, большие миоклонические и тонико-клонические припадки) по сравнению с этапом первичного обследования. Для всех включенных в исследование пациентов, принявших хотя бы 1 дозу ЛС, медиана снижения количества больших моторных припадков составила 32% у пациентов, получавших ламотриджин, и 9% — плацебо, что является статистически значимой разницей (p<0,05). Количество приступов внезапных падений значительно снижалось под действием ламотриджина (34%) по сравнению с плацебо (9%), также как и количество тонико-клонических припадков (снижение на 36% для ламотриджина по сравнению с увеличением на 10% для плацебо).
Дополнительная терапия ламотриджином у детей и взрослых пациентов с первично-генерализованными тонико-клоническими припадками. Эффективность применения ламотриджина в качестве дополнительной терапии у пациентов с первично-генерализованными тонико-клоническими припадками была установлена в многоцентровом двойном слепом плацебо-контролируемом исследовании с участием 117 детей и взрослых пациентов от 2 лет и старше (58 из них принимали ламотриджин, 59 — плацебо). Пациенты, имевшие не менее 3 первично-генерализованных тонико-клонических припадка в течение 8-недельного этапа первичного обследования, были рандомизированы на 19–24-недельное получение ламотриджина или плацебо дополнительно к текущей схеме лечения, включавшей применение до 2 противоэпилептических ЛС. Пациенты получали фиксированные дозы, целевые дозы варьировали от 3 до 12 мг/кг/сут для детей и от 200 до 400 мг/сут для взрослых пациентов с учетом сопутствующих противоэпилептических ЛС.
Первичной конечной точкой эффективности являлось процентное изменение количества первично-генерализованных тонико-клонических припадков по сравнению с этапом первичного обследования. Для всех включенных в исследование пациентов, принявших хотя бы 1 дозу ЛС, медиана процента снижения количества первично-генерализованных тонико-клонических припадков составила 66% у пациентов, получавших ламотриджин, и 34% у пациентов, получавших плацебо, что является статистически значимой разницей (p=0,006).
Биполярное расстройство
Эффективность применения ламотриджина в качестве поддерживающей терапии при биполярном расстройстве типа I была установлена в ходе 2 многоцентровых двойных слепых плацебо-контролируемых исследований с участием взрослых пациентов, отвечающих критериям биполярного расстройства типа I по определению DSM-IV (Diagnostic and Statistical Manual of Mental Disorders, 4th Edition). В исследование 1 были включены пациенты с текущим или недавним (в течение 60 дней) депрессивным эпизодом по определению DSM-IV, а в исследование 2 — пациенты с текущим или недавним (в течение 60 дней) эпизодом мании или гипомании по определению DSM-IV. Оба исследования включали когорту пациентов (30% из 404 пациентов в исследовании 1 и 28% из 171 пациентов в исследовании 2) с биполярным расстройством с быстрой цикличностью (от 4 до 6 эпизодов в год).
В обоих исследованиях дозу ламотриджина титровали до целевой 200 мг в качестве дополнительной терапии или монотерапии с постепенной отменой любых психотропных ЛС в течение 8–16 нед открытого периода (без контроля плацебо). В целом 81% из 1305 пациентов, принимавших участие в открытом периоде, получали 1 или более различных психотропных ЛС, включая бензодиазепины, СИОЗС, атипичные антипсихотики (включая оланзапин), вальпроат или литий, во время титрования дозы ламотриджина. Пациенты с оценкой тяжести расстройства 3 или менее по шкале общего клинического впечатления (шкала CGI), сохранявшейся в течение как минимум 4 последовательных недель, включая как минимум последнюю неделю монотерапии ламотриджином, были рандомизированы на плацебо-контролируемый двойной слепой период лечения продолжительностью до 18 мес. Первичной конечной точкой являлось время до вмешательства при эпизоде измененного настроения или до его возникновении, время до прекращения лечения либо из-за возникновения нежелательных реакций, которые были расценены как связанные с биполярным расстройством, либо из-за отсутствия эффективности. Эпизод расстройства настроения включал в себя депрессию, манию, гипоманию или являлся смешанным эпизодом настроения.
В двойном слепом исследовании 1 пациенты получали монотерапию ламотриджином в дозах 50 мг/сут (n=50), 200 мг/сут (n=124), 400 мг/сут (n=47) или плацебо (n=121). Ламотриджин (в группах лечения с дозой 200 и 400 мг/сут) превосходил плацебо по увеличению периода времени до наступления эпизода расстройства настроения. Раздельный анализ групп с дозой 200 и 400 мг/сут не выявил дополнительной пользы от приема более высокой дозы ламотриджина.
В двойном слепом исследовании 2 пациенты получали монотерапию ламотриджином (от 100 до 400 мг/сут, n=59) или плацебо (n=70). Ламотриджин превосходил плацебо по увеличению периода времени до возникновения эпизода расстройства настроения. Средняя доза ламотриджина составляла около 211 мг/сут.
Хотя результаты этих исследования изначально не предполагали раздельной оценки времени до наступления депрессии или мании, объединенный анализ двух исследований выявил статистически значимое преимущество ламотриджина перед плацебо в увеличении периода времени до наступления как депрессии, так и мании, однако результат для депрессии был более значимым.
Показания к применению
Эпилепсия
Дополнительная терапия при следующих типах припадков у пациентов от 2 лет и старше:
- парциальные припадки;
- первично-генерализованные тонико-клонические припадки;
- генерализованные припадки при синдроме Леннокса-Гасто.
Монотерапия (перевод на монотерапию пациентов от 16 лет и старше с парциальными припадками, которые получают лечение карбамазепином, фенитоином, фенобарбиталом, примидоном или вальпроатом в качестве единственного противоэпилептического ЛС. Безопасность и эффективность ламотриджина не установлены в качестве начальной монотерапии при переходе на нее с приема других противоэпилептических ЛС, кроме карбамазепина, фенитоина, фенобарбитала, примидона или вальпроата, при переходе на монотерапию с приема одновременно двух или более сопутствующих противоэпилептических ЛС.
Биполярное расстройство
В качестве поддерживающей терапии биполярного расстройства типа I с целью отсрочить наступление эпизодов расстройства настроения (депрессия, мания, гипомания, смешанные эпизоды) у пациентов от 18 лет и старше, получающих стандартную терапию для лечения острых эпизодов расстройства настроения. Эффективность ламотриджина при лечении острых эпизодов расстройства настроения не установлена. При назначении ламотриджина на срок, превышающий 16 нед, следует периодически проводить переоценку пользы долговременной терапии в каждом конкретном случае.
Противопоказания
Повышенная чувствительность (например, кожная сыпь, ангионевротический отек, острая крапивница, обширный зуд, изъязвление слизистой оболочки) к ламотриджину (см. «Меры предосторожности»).
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.
Как и в случае применения других противоэпилептических ЛС, физиологические изменения, происходящие во время беременности, могут повлиять на концентрацию ламотриджина и/или терапевтический эффект. Поступали сообщения о снижении концентрации ламотриджина во время беременности и восстановлении предродовых концентраций после родов. Для поддержания клинического ответа может потребоваться коррекция дозы.
Адекватных и хорошо контролируемых исследований с участием беременных женщин не проводилось. В исследованиях на животных ламотриджин оказывал токсическое воздействие на внутриутробное развитие в более низких дозах, чем при клиническом применении. Ламотриджин следует применять во время беременности только в том случае, если потенциальная польза для матери оправдывает потенциальный риск для плода.
При введении ламотриджина беременным мышам, крысам или кроликам в период органогенеза (пероральные дозы до 125, 25 и 30 мг/кг соответственно) у мышей и крыс наблюдалось снижение массы тела плода и увеличение частоты изменений скелета плода в дозах, которые также были токсичными для самок. Дозы отсутствия эффекта токсичности для эмбрионального развития у мышей, крыс и кроликов (75, 6,25 и 30 мг/кг соответственно) аналогичны (мыши и кролики) или меньше (крысы) дозы ламотриджина для человека 400 мг/сут в расчете на площадь поверхности тела.
В исследовании, в котором беременным крысам вводили ламотриджин (перорально в дозах 5 или 25 мг/кг) в период органогенеза, а потомство оценивали постнатально, у подвергавшегося воздействию потомства при обеих дозах наблюдались поведенческие отклонения. Наименьшая эффективная доза нейротоксического воздействия на внутриутробное развитие (отдаленная нейротоксичность) у крыс была ниже, чем доза ламотриджина для человека 400 мг/сут в расчете на площадь поверхности тела. Материнская токсичность наблюдалась при более высоких испытываемых дозах ламотриджина.
При введении ламотриджина беременным крысам (перорально в дозах 5, 10 или 20 мг/кг) на последних сроках беременности при всех дозах наблюдалась повышенная смертность потомства (включая мертворождение). Наименьшая эффективная доза токсического воздействия для пери-, постнатального развития у крыс ниже, чем доза ламотриджина для человека 400 мг/сут в расчете на площадь поверхности тела. Материнская токсичность наблюдалась при двух самых высоких дозах.
Ламотриджин снижает концентрацию фолатов в организме плода у крыс, что, как известно, связано с неблагоприятными исходами беременности у животных и человека.
Влияние применения ламотриджина на течение родов у человека неизвестно.
Ламотриджин присутствует в молоке кормящих женщин. Данные многочисленных небольших исследований показывают, что концентрация ламотриджина в плазме крови младенцев, находящихся на грудном вскармливании, достигает 50% от концентрации в плазме крови матери. Новорожденные и находящиеся на грудном вскармливании младенцы первого полугодия жизни подвергаются риску в связи с высокой концентрацией ламотриджина в плазме крови, поскольку после родов концентрация ламотриджина в плазме крови и молоке матери может иметь высокие показатели, если во время беременности доза ламотриджина была увеличена, но позже не снижена до дозировок, применяемых до беременности. Воздействие ламотриджина дополнительно увеличивается из-за несформировавшейся способности младенцев к глюкуронизации, необходимой для выведения ЛС. У младенцев, которых кормили грудным молоком матери, принимавшие ламотриджин, были зарегистрированы случаи развития апноэ, сонливости и плохого сосательного рефлекса, связь данных явлений с приемом ламотриджина не установлена. Следует внимательно наблюдать за состоянием младенцев, находящихся на грудном вскармливании, на предмет возникновения нежелательных реакций на ламотриджин. В случае возникновения опасений следует выяснить концентрацию ламотриджина в плазме крови младенца, чтобы исключить токсичность. Грудное вскармливание следует прекратить при наличии признаков токсичности ламотриджина.
Следует соблюдать осторожность при назначении ламотриджина женщинам в период грудного вскармливания.
Побочные действия
Опыт клинических исследований
Поскольку клинические исследования проводятся в различных условиях, частота возникновения нежелательных реакций, наблюдаемых в одном клиническом исследовании, не может напрямую сравниваться с частотой реакций в другом клиническом исследовании и может не отражать частоту, наблюдаемую на практике.
Эпилепсия
Дополнительная терапия у взрослых пациентов с эпилепсией. Наиболее часто наблюдавшимися (≥5% и чаще, чем при применении плацебо) побочными реакциями, связанными с применением ламотриджина в качестве дополнительной терапии у взрослых пациентов, были головокружение, атаксия, сонливость, головная боль, диплопия, нечеткость зрения, тошнота, рвота и кожная сыпь. Головокружение, диплопия, атаксия, нечеткость зрения, тошнота и рвота были дозозависимыми. Головокружение, диплопия, атаксия и нечеткость зрения чаще возникали у пациентов, получавших карбамазепин с ламотриджином, чем у пациентов, получавших другие противоэпилептические ЛС с ламотриджином. Клинические данные свидетельствуют о более высокой частоте возникновения кожной сыпи, включая тяжелую форму, у пациентов, получавших совместно ламотриджин и вальпроат, чем у пациентов, не получавших вальпроат (см. «Меры предосторожности»).
Примерно 11% из 3378 взрослых пациентов, получавших ламотриджин в качестве дополнительной терапии в клинических исследованиях, прекратили лечение из-за возникновения побочных реакций, наиболее частыми из которых были кожная сыпь (3%), головокружение (2,8%) и головная боль (2,5%).
В исследовании зависимости эффекта от дозы у взрослых пациентов частота прекращения приема ламотриджина из-за головокружения, атаксии, диплопии, нечеткости зрения, тошноты и рвоты зависела от дозы ламотриджина.
Монотерапия у взрослых пациентов с эпилепсией. Наиболее часто наблюдавшимися (≥5% и чаще, чем при применении плацебо) побочными реакциями, связанными с применением ламотриджина в виде монотерапии в контролируемом исследовании у взрослых пациентов были рвота, нарушение координации, диспепсия, тошнота, головокружение, ринит, беспокойство, бессонница, инфекции, боль, снижение массы тела, боль в груди и дисменорея. Наиболее часто наблюдаемыми (≥5% и чаще, чем при применении плацебо) побочными реакциями, связанными с применением ламотриджина в период перехода на монотерапию, были головокружение, головная боль, тошнота, астения, нарушение координации, рвота, кожная сыпь, сонливость, диплопия, атаксия, случайные травмы, тремор, нечеткость зрения, бессонница, нистагм, диарея, лимфаденопатия, зуд и синусит.
Примерно 10% из 420 взрослых пациентов, получавших ламотриджин в качестве монотерапии в клинических исследованиях, прекратили лечение из-за возникновения побочных реакций, наиболее частыми из которых были кожная сыпь (4,5%), головная боль (3,1%) и астения (2,4%).
Дополнительная терапия у детей и подростков с эпилепсией. Наиболее часто (≥5% и чаще, чем при применении плацебо) у детей и подростков от 2 до 16 лет наблюдались ассоциированные с применением ламотриджина инфекции, рвота, кожная сыпь, лихорадка, сонливость, случайные травмы, головокружение, диарея, абдоминальная боль (боль в животе), тошнота, атаксия, тремор, астения, бронхит, гриппоподобный синдром и диплопия, которые не отмечались с такой же частотой в контрольной группе.
Из 339 пациентов от 2 до 16 лет с парциальными или генерализованными припадками при синдроме Леннокса-Гасто из-за развития побочных реакций, наиболее частой из которых являлась кожная сыпь, лечение прекратили 4,2% пациентов, принимавших ламотриджин, и 2,9% пациентов, принимавших плацебо.
В другом исследовании примерно 11,5% из 1081 пациента от 2 до 16 лет, получавших ламотриджин в качестве дополнительной терапии в дорегистрационных клинических исследованиях, прекратили лечение из-за развития побочных реакций, наиболее частыми из которых являлись кожная сыпь (4,4%), обострение симптомов (1,7%) и атаксия (0,6%).
Контролируемые клинические исследования дополнительной терапии ламотриджином у взрослых пациентов с эпилепсией. В таблице 3 суммированы данные о побочных реакциях, которые наблюдались в ходе плацебо-контролируемых исследований у взрослых пациентов с эпилепсией, дополнительно получавших ламотриджин. В этих исследованиях дополнительно к текущей терапии противоэпилептическими ЛС пациенты получали ламотриджин или плацебо.
Таблица 3
Объединенные результаты плацебо-контролируемых исследований у взрослых пациентов с эпилепсией1,2
1 Побочные реакции, наблюдавшиеся не менее чем у 2% пациентов, получавших ламотриджин, и с большей частотой по сравнению с плацебо.
2 Пациенты в этих исследованиях получали от 1 до 3 сопутствующих противоэпилептических ЛС, таких как карбамазепин, фенитоин, фенобарбитал или примидон, в дополнение к ламотриджину или плацебо. Пациенты могли сообщать о множественных нежелательных реакциях, возникавших в ходе исследования или при прекращении лечения, таким образом, пациенты могли быть включены более чем в 1 категорию.
В рандомизированном исследовании с параллельными группами, в котором плацебо сравнивали с ламотриджином в дозах 300 и 500 мг/сут, некоторые из наиболее частых нежелательных реакций, связанных с приемом ЛС, были дозозависимыми (табл. 4).
Таблица 4
Дозозависимые побочные реакции, наблюдавшиеся в ходе рандомизированного плацебо-контролируемого исследования дополнительной терапии у взрослых пациентов с эпилепсией
1 Значительно больше, чем в группе плацебо (p<0,05).
2 Значительно больше, чем в группе, получавшей ламотриджин 300 мг (p<0,05).
Общий профиль побочных реакций, ассоциированных с применением ламотриджина, был аналогичен у женщин и мужчин и не зависел от возраста. Поскольку в плацебо-контролируемых исследованиях самая большая неевропеоидная расовая подгруппа составляла всего 6% пациентов, получавших ламотриджин, данных для подтверждения предположения о распределении сообщений о побочных реакциях в соответствии с расовой принадлежностью, недостаточно. Как правило, женщины, получавшие в качестве дополнительной терапии ламотриджин или плацебо, чаще сообщали о возникновении побочных реакций, чем мужчины. Единственной побочной реакцией, связанной с применением ламотриджина, сообщения о которой от женщин поступали более чем на 10% чаще, чем от мужчин (без соответствующего разделения по половому признаку в группе плацебо), было головокружение (различие 16,5%). Частота прекращения приема ламотриджина в связи с возникновением индивидуальных (отдельных) побочных реакций у женщин и мужчин различалась незначительно.
Контролируемое исследование монотерапии у взрослых пациентов с парциальными припадками. В таблице 5 приведены побочные реакции, наблюдавшиеся в двойном слепом исследовании у пациентов с эпилепсией, получавших монотерапию ламотриджином после отмены сопутствующего карбамазепина или фенитоина, и не наблюдавшиеся с такой же частотой в контрольной группе.
Таблица 5
Побочные реакции, наблюдавшиеся в ходе контролируемого исследования монотерапии у взрослых пациентов с парциальными припадками1,2
1 Побочные реакции, наблюдавшиеся по крайней мере у 5% пациентов, получавших ламотриджин, и с большей частотой, чем у получавших вальпроат.
2 Пациенты в данном исследовании были переведены на монотерапию ламотриджином или вальпроатом с дополнительной терапии карбамазепином или фенитоином. Пациенты могли сообщать о множественных нежелательных реакциях, возникавших в ходе исследования, и таким образом включены более чем в 1 категорию.
3 До 500 мг/сут.
4 1000 мг/сут.
Ниже приведены побочные реакции, отмечавшиеся с частотой более 2 и менее 5% у пациентов, получавших ламотриджин, и чаще, чем при приеме плацебо.
Со стороны организма в целом: астения, лихорадка.
Со стороны ЖКТ: анорексия, сухость во рту, ректальное кровотечение, пептическая язва.
Со стороны обмена веществ и питания: периферические отеки.
Со стороны нервной системы: амнезия, атаксия, депрессия, гипестезия, повышение либидо, снижение рефлексов/повышение рефлексов, нистагм, раздражительность, суицидальные мысли.
Со стороны дыхательной системы: носовое кровотечение, бронхит, одышка.
Со стороны кожи и подкожных тканей: контактный дерматит, сухость кожи, повышенная потливость.
Со стороны органов чувств: нарушения зрения.
Побочные реакции в контролируемых исследованиях по дополнительной терапии у детей и подростков с эпилепсией. В таблице 6 суммированы данные о побочных реакциях, наблюдавшихся у 339 детей и подростков с парциальными или генерализованными припадками при синдроме Леннокса-Гасто, получавших ламотриджин в дозе до 15 мг/кг/сут или максимально 750 мг/сут.
Таблица 6
Побочные реакции в объединенных плацебо-контролируемых дополнительных исследованиях у детей и подростков с эпилепсией1
1 Побочные реакции, наблюдавшиеся по крайней мере у 2% пациентов, получавших ламотриджин, и чаще, чем при приеме плацебо.
Биполярное расстройство
Наиболее частые побочные реакции, наблюдавшиеся в ходе 2 двойных слепых плацебо-контролируемых исследований продолжительностью 18 мес в связи с применением ламотриджина в качестве монотерапии (от 100 до 400 мг/сут) у взрослых пациентов (18 лет и старше) с биполярным расстройством, приведены в таблице 7. Побочные реакции, которые наблюдались по крайней мере у 5% пациентов и чаще на этапе повышения дозы ламотриджина в этих исследованиях (когда пациенты могли принимать сопутствующие ЛС), по сравнению с периодом монотерапии, были головная боль (25%), кожная сыпь (11%), головокружение (10%), диарея (8%), нарушение сна (6%) и зуд (6%).
На этапе монотерапии в двойном слепом плацебо-контролируемом исследовании продолжительностью 18 мес 13% из 227 пациентов, получавших ламотриджин (от 100 до 400 мг/сут), 16% из 190 пациентов, получавших плацебо, и 23% из 166 пациентов, получавших литий, прекратили лечение из-за возникновения побочных реакций, наиболее частыми из которые были кожная сыпь (3%) и мания/гипомания/смешанные эпизоды измененного настроения (2%). Приблизительно 16% из 2401 пациента, принимавшего ламотриджин (от 50 до 500 мг/сут) для лечения биполярного расстройства в дорегистрационных исследованиях, прекратили терапию из-за возникновения побочных реакций, чаще всего из-за кожной сыпи (5%) и мании/гипомании/смешанных эпизодов измененного настроения (2%).
Общий профиль нежелательных реакций на ламотриджин был схож у женщин и мужчин, молодых пациентов и пациентов пожилого возраста, а также у представителей разных расовых групп.
Таблица 7
Побочные реакции, наблюдавшиеся в ходе 2 плацебо-контролируемых исследований у взрослых пациентов с биполярным расстройством типа I1,2
1 Побочные реакции, наблюдавшиеся не менее чем у 5% пациентов, получавших ламотриджин, и чаще, чем при приеме плацебо.
2 Пациенты в этих исследованиях были переведены на монотерапию ламотриджином (от 100 до 400 мг/сут) или плацебо после дополнительной терапии другими психотропными ЛС. Пациенты могли сообщать о множественных нежелательных реакциях, возникавших в ходе исследования и таким образом включены более чем в 1 категорию.
3 В общих клинических исследованиях биполярных и других аффективных расстройств частота возникновения тяжелой формы кожной сыпи составляла 0,08% (1 из 1233) у взрослых пациентов, получавших ламотриджин в качестве начальной монотерапии, и 0,13% (2 из 1538) у взрослых пациентов, получавших ламотриджин в качестве дополнительной терапии (см. «Меры предосторожности»).
Другие реакции, которые наблюдались у 5% или более пациентов, но в равной степени или чаще в группе плацебо, включали головокружение, манию, головную боль, инфекции, грипп, боль, случайные травмы, диарею и диспепсию.
С частотой более 1 и менее 5% у пациентов, получавших ламотриджин, и чаще, чем при приеме плацебо, отмечались следующие побочные реакции.
Со стороны организма в целом: лихорадка, боль в шее.
Со стороны ССС: мигрень.
Со стороны ЖКТ: метеоризм.
Со стороны обмена веществ и питания: повышение массы тела, отеки.
Со стороны опорно-двигательного аппарата: артралгия, миалгия.
Со стороны нервной системы: амнезия, депрессия, возбуждение, эмоциональная неустойчивость (лабильность), диспраксия, расстройства мышления, нарушения сна, гипестезия.
Со стороны дыхательной системы: синусит.
Со стороны мочеполовой системы: частое мочеиспускание.
Побочные реакции, возникавшие после резкой отмены приема ламотриджина. В 2 исследованиях поддерживающей терапии не отмечалось увеличения частоты, тяжести или типа побочных реакций у пациентов с биполярным расстройством после резкой отмены приема ламотриджина. В клинических исследованиях у пациентов с биполярным расстройством у 2 пациентов наблюдались судорожные припадки вскоре после резкой отмены приема ламотриджина. Однако наличие отягощающих факторов также могло способствовать возникновению судорожных припадков у этих пациентов с биполярным расстройством (см. «Меры предосторожности»).
Мания/гипомания/смешанные эпизоды измененного настроения. В ходе двойных слепых плацебо-контролируемых клинических исследований биполярного расстройства типа I, в которых пациенты были переведены на монотерапию ламотриджином (от 100 до 400 мг/сут) после приема других психотропных ЛС и наблюдались в течение 18 мес, частота маниакальных, гипоманиакальных или смешанных эпизодов измененного настроения, зарегистрированных в качестве побочных реакций, составила 5% для пациентов, получавших ламотриджин (n=227), 4% для пациентов, получавших литий (n=166), и 7% для пациентов, получавших плацебо (n=190). Во всех контролируемых исследованиях биполярного расстройства суммарно побочные реакции мании (включая гипоманию и смешанные эпизоды измененного настроения) были зарегистрированы у 5% пациентов, получавших ламотриджин (n=956), 3% пациентов, получавших литий (n=280), и 4% пациентов, получавших плацебо (n=803).
Другие побочные реакции, наблюдавшиеся во всех клинических исследованиях
Полные данные о побочных реакциях, возникавших в ходе всех клинических исследований, только некоторые из которых были плацебо-контролируемыми, собраны по 6694 пациентам, получавшим ламотриджин.
В ходе этих исследований все побочные реакции регистрировались клиническими исследователями с использованием терминологии по их собственному выбору. Для достоверной оценки доли лиц с побочными реакциями схожего типа эти реакции были сгруппированы в соответствии с модифицированной терминологией словаря COSTART. Представленная частота побочных реакций отражает долю от 6694 пациентов, получавших ламотриджин, которые испытали событие указанного типа по крайней мере 1 раз во время его приема. Включены все зарегистрированные побочные реакции, за исключением уже перечисленных в вышеприведенных таблицах или упоминавшихся в других разделах, приведенных в слишком общих неинформативных формулировках и обоснованно не связанных с применением ламотриджина.
Побочные реакции приведены ниже по категориям систем органов и перечислены в порядке уменьшения частоты их встречаемости, используя следующие определения: часто (побочные реакции наблюдаются у не менее 1/100 пациентов); нечасто (побочные реакции наблюдаются у менее 1/100 до не менее 1/1000 пациентов); редко (нежелательные реакции наблюдаются у менее 1/1000 пациентов).
Со стороны организма в целом: нечасто — аллергические реакции, озноб, общее недомогание.
Со стороны ССС: нечасто — приливы крови к лицу, приливы жара (климактерический синдром), гипертония, ощущение сердцебиения, постуральная гипотензия, обморок, тахикардия, вазодилатация.
Со стороны кожи: нечасто — акне, алопеция, гирсутизм (избыточное оволосение у женщин), макулопапулезная сыпь, изменение или потеря цвета кожи, крапивница; редко — ангионевротический отек, эритема, эксфолиативный дерматит, грибковый дерматит, опоясывающий герпес, лейкодерма, мультиформная эритема, петехиальная сыпь, пустулезная сыпь, синдром Стивенса-Джонсона, везикулезно-буллезная сыпь.
Со стороны пищеварительной системы: нечасто — дисфагия, отрыжка, гастрит, гингивит, повышенный аппетит, повышенное слюноотделение, отклонения в функциональных печеночных пробах, язвенный стоматит; редко — желудочно-кишечное кровотечение, глоссит, кровоточивость десен, гиперплазия десен, гематемезис (кровавая рвота), геморрагический колит, гепатит, мелена, язва желудка, стоматит, отек языка.
Со стороны эндокринной системы: редко — зоб, гипотиреоз.
Со стороны крови и лимфатической системы: нечасто — экхимоз (подкожное кровоизлияние), лейкопения; редко — анемия, эозинофилия, снижение фибрина, снижение фибриногена, железодефицитная анемия, лейкоцитоз, лимфоцитоз, макроцитарная анемия, петехия, тромбоцитопения.
Со стороны обмена веществ и питания: нечасто — повышение уровня АСТ; редко — непереносимость алкоголя, повышение уровня ЩФ, АЛТ, билирубинемия, общие отеки, повышение ГГТП, гипергликемия.
Со стороны скелетно-мышечной системы: нечасто — артрит, судороги ног, миастения, подергивания (судорожные движения); редко — бурсит, атрофия мышц, патологические переломы, контрактура сухожилий.
Со стороны нервной системы: часто — спутанность сознания, парестезия; нечасто — акатизия, апатия, афазия, угнетение ЦНС, деперсонализация, дизартрия, дискинезия, эйфория, галлюцинации, проявление враждебности, гиперкинезия, гипертония, снижение либидо, расстройства памяти, скачкообразное мышление, двигательные расстройства, миоклонические судороги (миоклония), панические атаки, параноидальные реакции, расстройство личности (психопатия), психоз, нарушения сна, ступор, суицидальные мысли; редко — хореоатетоз, делирий, бред (бредовые идеи), дисфория, дистония, экстрапирамидный синдром, обморок (потеря сознания), большие судорожные припадки, гемиплегия, гипералгезия, гиперестезия, гипокинезия, гипотония, маниакально-депрессивные реакции, мышечные спазмы, невралгия, невроз, паралич, периферический неврит.
Со стороны органов дыхания: нечасто — зевота; редко — икота, гипервентиляция легких.
Со стороны органов чувств: часто — амблиопия; нечасто — нарушение аккомодации, конъюнктивит, сухость глаз, боль в ушах, светобоязнь, дисгевзия (извращение вкуса), шум в ушах; редко — глухота (тугоухость), нарушение слезоотделения, осциллопсия, паросмия, птоз, косоглазие, потеря вкуса, увеит, дефекты поля зрения.
Со стороны мочеполовой системы: нечасто — нарушение эякуляции, гематурия, импотенция, меноррагия, полиурия, недержание мочи; редко — острая почечная недостаточность, аноргазмия, абсцесс молочной железы, неоплазия молочной железы, повышение креатинина, цистит, дизурия, эпидидимит, выделения из молочных желез, почечная недостаточность, боль в почках, никтурия, задержка мочеиспускания, неотложные позывы к мочеиспусканию.
Результаты пострегистрационного наблюдения
В ходе применения ламотриджина в пострегистрационный период были выявлены следующие побочные реакции (не перечисленные выше в клинических исследованиях или других информационных разделах). Поскольку эти данные получены из спонтанных сообщений от популяции неопределенного размера, невозможно достоверно оценить их частоту возникновения или установить причинно-следственную связь с воздействием ламотриджина.
Со стороны крови и лимфатической системы: агранулоцитоз, гемолитическая анемия, лимфаденопатия, не связанная с нарушениями гиперчувствительности.
Со стороны ЖКТ: эзофагит.
Со стороны гепатобилиарного тракта и поджелудочной железы: панкреатит.
Со стороны иммунной системы: волчаночноподобный синдром, васкулит.
Со стороны нижних дыхательных путей: апноэ.
Со стороны опорно-двигательного аппарата: рабдомиолиз наблюдался у пациентов с реакциями гиперчувствительности.
Со стороны нервной системы: агрессия, обострение симптомов Паркинсона у пациентов с уже существующей болезнью Паркинсона, тики.
Нелокализованные: прогрессирующая иммуносупрессия.
Взаимодействие
Фармакокинетические данные по лекарственному взаимодействию
На кажущийся клиренс ламотриджина влияет совместное применение некоторых ЛС (см. «Меры предосторожности», «Взаимодействие»).
Данные о ФКВ ламотриджина и других ЛС представлены в таблице 8.
Таблица 8
Обобщенные данные о взаимодействии других ЛС и ламотриджина
1 По данным дополнительных клинических исследований и исследований с участием добровольцев.
2 Совокупный эффект оценивался путем сравнения средних значений клиренса, полученных в ходе дополнительных клинических исследований и исследований с участием добровольцев.
3 Влияние других гормональных контрацептивов или ЗГТ на фармакокинетику ламотриджина в клинических исследованиях систематически не оценивалось, хотя эффект может быть аналогичен наблюдаемому при применении комбинации этинилэстрадиол + левоноргестрел.
4 Незначительное снижение концентрации левоноргестрела.
5 Незначительное снижение, клинически значимого эффекта не ожидается.
6 По сравнению с показателями групп исторического контроля.
7 Не назначается, но является активным метаболитом карбамазепина.
8 Не назначается, но является активным метаболитом окскарбазепина.
9 Не назначается, но является активным метаболитом рисперидона.
10 Незначительное увеличение, клинически значимого эффекта не ожидается.
Условные обозначения: ↔ — отсутствие значительного эффекта, ↓ — снижение концентрации, ↑ — увеличение концентрации, ? — противоречивые данные.
Эстрогенсодержащие пероральные контрацептивы. У 16 женщин-добровольцев прием пероральных контрацептивов, содержащих 30 мкг этинилэстрадиола и 150 мкг левоноргестрела, повышал кажущийся клиренс ламотриджина (300 мг/сут) примерно в 2 раза со средним снижением AUC на 52% и Cmax на 39%. В данном исследовании концентрация ламотриджина в сыворотке крови постепенно повышалась и была в среднем примерно в 2 раза выше в конце недели приема неактивного гормонального препарата по сравнению с таковой в конце активного гормонального цикла.
Постепенное транзиторное повышение концентрации ламотриджина в плазме крови (приблизительно 2-кратное увеличение) происходило в течение недели без таблеток у женщин, которые не принимали также ЛС, повышающие клиренс ламотриджина (карбамазепин, фенитоин, фенобарбитал, примидон или другие ЛС, такие как рифампицин и ингибиторы протеазы лопинавир + ритонавир и атазанавир + ритонавир, индуцирующие глюкуронизацию ламотриджина). Повышение концентрации ламотриджина в плазме крови будет более значительным, если дозу ламотриджина увеличить за несколько дней до или в течение недели без таблеток. Повышение концентрации ламотриджина в плазме крови может привести к возникновению дозозависимых побочных реакций.
В том же исследовании совместное применение ламотриджина (300 мг/сут) у 16 женщин-добровольцев не повлияло на фармакокинетику этинилэстрадиола в комбинированном пероральном контрацептивном ЛС. Наблюдалось среднее снижение AUC и Cmax на 19 и 12% соответственно. Измерение уровня прогестерона в сыворотке крови показало, что ни у одного из 16 добровольцев не было гормональных признаков овуляции, хотя измерение уровня ФСГ, ЛГ и эстрадиола в сыворотке крови указывало на некоторую потерю подавления гипоталамо-гипофизарно-яичниковой оси.
Эффекты доз ламотриджина, отличных от 300 мг/сут, в контролируемых клинических исследованиях систематически не оценивались.
Клиническое значение наблюдаемых гормональных изменений на овуляторную активность неизвестно. Однако нельзя исключить возможность снижения контрацептивной эффективности у некоторых пациентов. Поэтому пациентки должны быть проинструктированы о необходимости незамедлительно сообщать лечащему врачу об изменениях в менструальном цикле (например, о прорывных кровотечениях).
Для женщин, принимающих эстрогенсодержащие пероральные контрацептивы, может потребоваться коррекция дозы ламотриджина.
Другие гормональные контрацептивы или ЗГТ. Влияние других гормональных контрацептивов или ЗГТ на фармакокинетику ламотриджина систематически не оценивалось. Сообщалось, что этинилэстрадиол, а не прогестагены, увеличивал клиренс ламотриджина в 2 раза, а таблетки, содержащие только прогестины, не влияли на концентрацию ламотриджина в плазме крови. Поэтому коррекция дозы ламотриджина в присутствии только прогестагенов, скорее всего, не потребуется.
Арипипразол. У 18 пациентов с биполярным расстройством со схемой регулярного приема ламотриджина в дозе от 100 до 400 мг/сут AUC и Cmax ламотриджина были снижены примерно на 10% у пациентов, которые получали арипипразол от 10 до 30 мг/сут в течение 7 дней, а затем 30 мг/сут в течение дополнительных 7 дней. Такое снижение экспозиции ламотриджина не считается клинически значимым.
Комбинация атазанавир + ритонавир. В исследовании с участием здоровых добровольцев суточные дозы комбинации атазанавир + ритонавир (300 мг/100 мг) снижали AUC и Cmax ламотриджина в плазме крови (однократная доза 100 мг) в среднем на 32 и 6% соответственно и сокращали T1/2 на 27%. При совместном применении комбинации атазанавир + ритонавир (300 мг/100 мг) соотношение метаболитов к ламотриджину увеличивалось с 0,45 до 0,71, что соответствует индукции глюкуронизации. Фармакокинетика комбинации атазанавир + ритонавир в присутствии сопутствующего ламотриджина была аналогична таковой в отсутствие ламотриджина в группах исторического контроля.
Бупропион. Фармакокинетика при приеме однократной дозы ламотриджина 100 мг у здоровых добровольцев (n=12), получавших бупропион в лекарственной форме с замедленным высвобождением (150 мг 2 раза в день) в течение 11 дней до приема ламотриджина, не изменялась.
Карбамазепин. Прием ламотриджина не оказывает заметного влияния на Css карбамазепина в плазме крови. Ограниченные клинические данные свидетельствуют о более высокой частоте возникновения головокружения, диплопии, атаксии и нечеткости зрения у пациентов, получающих совместно карбамазепин и ламотриджин, чем у пациентов, получающих другие противоэпилептические ЛС с ламотриджином. Механизм этого взаимодействия не совсем ясен. Влияние ламотриджина на концентрацию карбамазепина эпоксида в плазме крови не выяснено. У небольшой группы пациентов (n=7), принимавших участие в плацебо-контролируемом исследовании, прием ламотриджина не влиял на концентрацию карбамазепина эпоксида в плазме крови, но в небольшом неконтролируемом исследовании (n=9) концентрация карбамазепина эпоксида повышалась.
Сопутствующее применение карбамазепина снижает Css ламотриджина примерно на 40%.
Фелбамат. В исследовании с участием 21 здорового добровольца совместное применение фелбамата (1200 мг 2 раза в день) с ламотриджином (100 мг 2 раза в день в течение 10 дней) не оказало клинически значимого влияния на фармакокинетику ламотриджина.
Ингибиторы фолатов. Ламотриджин является слабым ингибитором дигидрофолатредуктазы, что следует учитывать при назначении других ЛС, ингибирующих метаболизм фолатов.
Габапентин. На основании ретроспективного анализа концентрации в плазме крови у 34 пациентов, получавших ламотриджин как с габапентином, так и без него, габапентин, по-видимому, не изменяет кажущийся клиренс ламотриджина.
Леветирацетам. Потенциальное лекарственное взаимодействие леветирацетама и ламотриджина оценивалось в ходе плацебо-контролируемых клинических исследований исходя из показателей концентрации обоих ЛС в плазме крови. Согласно полученным данным, ламотриджин не влияет на фармакокинетику леветирацетама, а леветирацетам не влияет на фармакокинетику ламотриджина.
Литийсодержащие ЛС. Фармакокинетика лития не изменялась у здоровых добровольцев (n=20) при совместном применении с ламотриджином (100 мг/сут) в течение 6 дней.
Комбинация лопинавир + ритонавир. У 18 здоровых добровольцев добавление лопинавира (400 мг 2 раза в день) и ритонавира (100 мг 2 раза в день) снижало AUC, Cmax и T1/2 ламотриджина приблизительно на 50–55,4%. Фармакокинетика лопинавира и ритонавира не изменялась при сопутствующем применении ламотриджина по сравнению с таковой в группах исторического контроля.
Оланзапин. AUC и Cmax оланзапина были сходными после его совместного применения (15 мг 1 раз в день) с ламотриджином (200 мг 1 раз в день) у здоровых мужчин-добровольцев (n=16) по сравнению с AUC и Cmax у здоровых мужчин-добровольцев, получавших только оланзапин (n=16).
В том же исследовании AUC и Cmax ламотриджина снижались в среднем на 24 и 20% соответственно после добавления оланзапина к ламотриджину у здоровых мужчин-добровольцев по сравнению с монотерапией ламотриджином. Ожидается, что такое снижение концентрации ламотриджина в плазме крови не будет иметь клинического значения.
Окскарбазепин. AUC и Cmax окскарбазепина и его активного метаболита 10-моногидроксиокскарбазепина после совместного применения окскарбазепина (600 мг 2 раза в день) и ламотриджина (200 мг 1 раз в день) у здоровых мужчин-добровольцев (n=13) не отличались существенно от таковых у здоровых мужчин-добровольцев, получавших только окскарбазепин (n=13).
В том же исследовании AUC и Cmax ламотриджина после сопутствующего применения окскарбазепина (600 мг 2 раза в день) у здоровых мужчин-добровольцев были сходными с таковыми у тех, кто получал только ламотриджин. Ограниченные клинические данные свидетельствуют о более высокой частоте возникновения головной боли, головокружения, тошноты и сонливости при одновременном применении ламотриджина и окскарбазепина по сравнению с применением только ламотриджина или только окскарбазепина.
Фенобарбитал, примидон. Совместное применение фенобарбитала или примидона снижает Css ламотриджина в плазме крови приблизительно на 40%.
Фенитоин. Прием ламотриджина не оказывает заметного влияния на Css фенитоина в плазме крови у пациентов с эпилепсией. Css ламотриджина в плазме крови снижается приблизительно на 40% при совместном применении фенитоина.
Прегабалин. Одновременное применение прегабалина (200 мг 3 раза в день) не влияет на Css ламотриджина в плазме крови. ФКВ между ламотриджином и прегабалином отсутствует.
Рифампицин. У 10 мужчин-добровольцев прием рифампицина (600 мг/сут в течение 5 дней) увеличил кажущийся клиренс ламотриджина после приема однократной дозы 25 мг приблизительно в 2 раза (AUC уменьшалась приблизительно на 40%).
Рисперидон. В исследовании с участием 14 здоровых добровольцев многократный прием ламотриджина в дозе 400 мг ежедневно не оказывал клинически значимого влияния на фармакокинетику однократной дозы рисперидона 2 мг и его активного метаболита 9-гидроксирисперидона. После одновременного применения рисперидона в дозе 2 мг и ламотриджина у 12 из 14 добровольцев отмечалась сонливость по сравнению с 1 из 20 добровольцев, принимавших только рисперидон, и ни у одного добровольца, принимавшего только ламотриджин.
Топирамат. Прием топирамата не приводит к изменению концентрации ламотриджина в плазме крови. Ламотриджин повышает концентрацию топирамата на 15%.
Вальпроат. При назначении ламотриджина здоровым добровольцам (n=18), принимавшим вальпроат, Cmin вальпроата в плазме крови в равновесном состоянии снижалась в среднем на 25% в течение 3 нед, а затем стабилизировалась. Однако в контролируемых клинических исследованиях добавление ламотриджина к проводимой терапии не вызывало изменения концентрации вальпроата в плазме крови ни у взрослых, ни у детей.
Добавление вальпроата повышало Сss ламотриджина у здоровых добровольцев чуть более чем в 2 раза. В одном исследовании максимальное ингибирование клиренса ламотриджина было достигнуто при дозах вальпроата от 250 до 500 мг/сут и не увеличивалось при дальнейшем повышении дозы вальпроата.
Зонисамид. В исследовании с участием 18 пациентов с эпилепсией одновременное применение зонисамида (200–400 мг/сут) и ламотриджина (150–500 мг/сут в течение 35 дней) не оказывало существенного влияния на фармакокинетику ламотриджина.
Известные индукторы или ингибиторы глюкуронизации. ЛС, кроме перечисленных выше, не подвергались систематической оценке в комбинации с ламотриджином. Поскольку ламотриджин метаболизируется преимущественно путем конъюгации глюкуроновой кислоты, ЛС, которые индуцируют или ингибируют глюкуронизацию, могут повлиять на кажущийся клиренс ламотриджина и может потребоваться коррекция дозы ламотриджина в зависимости от клинического ответа.
Другие ЛС. Ламотриджин является ингибитором почечной канальцевой секреции, опосредованной OCT2. Оценка in vitro ингибирующего действия ламотриджина на OCT2 показала, что ламотриджин, но не метаболит N-2-глюкуронид, в потенциально клинически значимых концентрациях является ингибитором OCT2, со значением IC50 53,8 мкмоль/л. Это может привести к увеличению концентрации в плазме крови некоторых ЛС, которые в значительной степени экскретируются этим путем. Совместное применение ламотриджина и субстратов OCT2 с узким терапевтическим индексом (например, дофетилид) не рекомендуется.
Результаты экспериментов in vitro показывают, что маловероятно снижение клиренса ламотриджина при одновременном применении с амитриптилином, клоназепамом, клозапином, флуоксетином, галоперидолом, лоразепамом, фенелзином, сертралином или тразодоном.
Результаты экспериментов in vitro свидетельствуют о том, что ламотриджин не снижает клиренс ЛС, элиминируемых преимущественно CYP2D6.
Передозировка
Симптомы: сообщалось о случаях передозировки ламотриджина в дозах до 15 г, некоторые из которых приводили к летальному исходу. Передозировка приводила к атаксии, нистагму, судорогам (включая тонико-клонические судороги), снижению уровня сознания, коме и задержке внутрижелудочковой проводимости.
Лечение: специфического антидота не существует. При подозрении на передозировку ламотриджина рекомендуется госпитализация пациента. Показана общая поддерживающая терапия, включая частый мониторинг жизненно важных показателей и тщательное наблюдение за состоянием пациента. При наличии показаний следует индуцировать рвоту, необходимо принять обычные меры предосторожности для защиты дыхательных путей. Следует иметь в виду, что ламотриджин в лекарственной форме с немедленным высвобождением быстро всасывается. Неясно, является ли гемодиализ эффективным средством выведения ламотриджина из крови. У 6 пациентов с почечной недостаточностью около 20% ламотриджина удалялось путем гемодиализа в течение 4-часового сеанса.
Способ применения и дозы
Перорально, режим дозирования и продолжительность применения зависят от показания и клинического состояния пациента и устанавливаются врачом.
Меры предосторожности
Тяжелые формы кожной сыпи
Дети. Частота возникновения тяжелой формы кожной сыпи, связанной с госпитализацией и прекращением приема ламотриджина в проспективно наблюдаемой когорте педиатрических пациентов (от 2 до 16 лет) с эпилепсией, получавших дополнительную терапию, составила приблизительно 0,8% (16 из 1983 пациентов). При оценке 14 из этих случаев тремя экспертами-дерматологами возникли значительные разногласия относительно правильности их классификации. Например, один дерматолог не отнес ни один из случаев к синдрому Стивенса-Джонсона, другой поставил этот диагноз в 7 из 14 случаев. В этой когорте из 1983 пациентов был зарегистрирован 1 случай с летальным исходом, ассоциированный с возникновением кожной сыпи. Кроме того, в американском и зарубежном пострегистрационном опыте применения ламотриджина наблюдались редкие случаи развития токсического эпидермального некролиза с необратимыми последствиями и/или летальным исходом или без них.
Имеются данные, доказывающие, что включение вальпроата в схему лечения несколькими ЛС повышает риск развития тяжелой, потенциально опасной для жизни формы кожной сыпи у педиатрических пациентов. У детей, одновременно принимавших вальпроат, в 1,2% (6 из 482) случаев наблюдалась тяжелая форма кожной сыпи по сравнению с 0,6% (6 из 952) пациентов, не принимавших вальпроат.
Взрослые. Тяжелая форма кожной сыпи, связанная с госпитализацией и прекращением приема ламотриджина, возникала у 0,3% (11 из 3348) взрослых пациентов, получавших ламотриджин в дорегистрационных клинических исследованиях эпилепсии. В клинических исследованиях биполярных и других аффективных расстройств частота возникновения тяжелой формы кожной сыпи составляла 0,08% (1 из 1233) у взрослых пациентов, получавших ламотриджин в качестве начальной монотерапии, и 0,13% (2 из 1538) у взрослых пациентов, получавших ламотриджин в качестве дополнительной терапии. Смертельных случаев среди этих пациентов не зарегистрировано. Однако в мировом пострегистрационном опыте применения ламотриджина сообщалось о редких случаях с летальным исходом, ассоциированных с возникновением кожной сыпи, но их количество слишком мало, чтобы точно оценить частоту.
Среди кожных высыпаний, приводивших к госпитализации, отмечались синдром Стивенса-Джонсона, токсический эпидермальный некролиз, ангионевротический отек и высыпания, связанные с синдромом лекарственной гиперчувствительности.
Имеются данные, доказывающие, что включение вальпроата в схему лечения несколькими ЛС повышает риск развития тяжелой, потенциально опасной для жизни формы кожной сыпи у взрослых пациентов. В частности, из 584 пациентов, принимавших ламотриджин в комбинации с вальпроатом в клинических исследованиях эпилепсии, 6 пациентов (1%) были госпитализированы в связи с возникновением кожной сыпи, в отличие от 4 (0,16%) госпитализированных из 2398 пациентов и добровольцев, принимавших ламотриджин в качестве монотерапии (без вальпроата).
Пациенты с аллергическими реакциями или кожной сыпью на другие противоэпилептические ЛС в анамнезе. Риск возникновения незначительных кожных высыпаний (легкая форма кожной сыпи) повышается при превышении рекомендуемой начальной дозы и/или предписанных темпов увеличения дозы ламотриджина, а также у пациентов с аллергическими реакциями или кожной сыпью на другие противоэпилептические ЛС в анамнезе.
Синдромом лекарственной гиперчувствительности и полиорганная недостаточность
При приеме ламотриджина наблюдался синдром лекарственной гиперчувствительности, также известный как лекарственная реакция с эозинофилией и системными симптомами (DRESS-синдром). Некоторые из этих реакций были жизнеугрожающими или с летальным исходом. DRESS-синдром чаще всего проявляется лихорадкой, кожной сыпью и/или лимфаденопатией в сочетании с поражением других систем органов, такими как гепатит, нефрит, гематологические нарушения, миокардит или миозит, иногда напоминающие острую вирусную инфекцию. Часто присутствует эозинофилия. Выраженность этого заболевания различна, и в него могут быть вовлечены другие, не упомянутые ранее, системы органов.
Летальные исходы, связанные с острой полиорганной недостаточностью и печеночной недостаточностью различной степени тяжести, были зарегистрированы у 2 из 3796 взрослых пациентов и 4 из 2435 педиатрических пациентов, получавших ламотриджин в клинических исследованиях эпилепсии. Также сообщалось о редких случаях летального исхода от полиорганной недостаточности в пострегистрационный период применении ламотриджина.
При применении ламотриджина также сообщалось о случаях возникновения только печеночной недостаточности — без кожной сыпи или поражения других органов.
Важно отметить, что ранние проявления гиперчувствительности (например, лихорадка, лимфаденопатия) могут наблюдаться даже при отсутствии кожной сыпи. Следует провести немедленное обследование пациента, если присутствуют такие признаки или симптомы. Если установить альтернативную этиологию признаков или симптомов невозможно, прием ламотриджина следует отменить.
Перед началом терапии ламотриджином пациентов следует информировать о том, что возникновение кожной сыпи или появление других признаков или симптомов гиперчувствительности (например, лихорадка, лимфаденопатия) могут являться предвестниками серьезного заболевания и о них следует немедленно сообщать лечащему врачу.
Дискразия крови
Имеются сообщения о случаях развития дискразии крови, которые могли или не могли быть связаны с DRESS-синдромом. К ним относятся нейтропения, лейкопения, анемия, тромбоцитопения, панцитопения и, в редких случаях, апластическая анемия и истинная эритроцитарная аплазия.
Суицидальные мысли или поведение
Противоэпилептические ЛС, включая ламотриджин, повышают риск возникновения суицидальных мыслей или поведения у пациентов, принимающих эти ЛС по любым показаниям. Пациенты, получающие терапию любым противоэпилептическим ЛС по любому показанию, должны наблюдаться на предмет появления или обострения депрессии, суицидальных мыслей или поведения и/или любых необычных изменений настроения или поведения.
Объединенный анализ 199 плацебо-контролируемых клинических исследований (монотерапия и дополнительная терапия) 11 различных противоэпилептических ЛС показал, что у пациентов, рандомизированных для приема одного из противоэпилептических ЛС, риск возникновения суицидальных мыслей или поведения был примерно в 2 раза выше (скорректированный ОР 1,8; 95% ДИ: 1,2; 2,7) по сравнению с пациентами, рандомизированными для приема плацебо. В этих исследованиях со средней продолжительностью лечения 12 нед предполагаемая частота суицидального поведения или мыслей среди 27863 пациентов, получавших противоэпилептические ЛС, составила 0,43% по сравнению с 0,24% среди 16029 пациентов, получавших плацебо, что представляет собой увеличение приблизительно на 1 случай появления суицидальных мыслей или поведения на каждые 530 пациентов, получавших лечение. В ходе исследований было зарегистрировано 4 случая самоубийства среди пациентов, получавших противоэпилептические ЛС, и ни одного у пациентов, получавших плацебо, но количество случаев слишком мало, чтобы можно было сделать вывод о влиянии приема противоэпилептических ЛС на самоубийство.
Повышенный риск возникновения суицидальных мыслей или поведения при терапии противоэпилептическими ЛС наблюдался уже через 1 нед после начала лечения и сохранялся в течение всего оцениваемого периода лечения. Поскольку продолжительность большинства исследований, включенных в анализ, не превышала 24 нед, не представляется возможным оценить риск возникновения суицидальных мыслей или поведения после 24 нед.
Согласно анализу данных, риски возникновения суицидальных мыслей или поведения в целом были идентичны для ЛС, применяемых в исследованиях. Обнаружение повышенного риска при применении противоэпилептических ЛС с различным механизмом действия и по целому ряду показаний позволяет предположить, что этот риск распространяется на все противоэпилептические ЛС, применяемые по любому показанию. В проанализированных клинических исследованиях риск существенно не варьировал по возрасту (от 5 до 100 лет).
ОР возникновения суицидальных мыслей или поведения был выше в клинических исследованиях по эпилепсии, чем в клинических исследованиях по психическим или другим расстройствам, но разница в абсолютном риске была одинаковой для показаний по эпилепсии и психическим расстройствам.
Перед назначением ламотриджина или любого другого противоэпилептического ЛС следует сопоставить риск возникновения суицидальных мыслей или поведения с риском нелеченого заболевания. Эпилепсия и многие другие заболевания, для лечения которых назначаются противоэпилептические ЛС, сами по себе связаны с заболеваемостью и смертностью, а также с повышенным риском возникновения суицидальных мыслей и поведения. При возникновении суицидальных мыслей или поведения во время терапии противоэпилептическими ЛС в каждом конкретном случае лечащий врач должен оценить возможную связь появления этих симптомов с самим заболеванием.
Пациенты, их опекуны или члены семьи должны быть проинформированы о том, что прием противоэпилептических ЛС повышает риск возникновения суицидальных мыслей и поведения, и предупреждены о необходимости быть бдительными при появлении или обострении признаков и симптомов депрессии, любых необычных изменений настроения или поведения, появлении суицидальных мыслей или поведения, или мыслей о причинении физического вреда собственному телу (самоповреждение). О поведении, вызывающем беспокойство, следует немедленно сообщать лечащему врачу.
Биполярное расстройство
Лечение острых эпизодов расстройства настроения. Безопасность и эффективность применения ламотриджина при лечении острых эпизодов расстройства настроения не установлены.
Дети и подростки (младше 18 лет). Безопасность и эффективность применения ламотриджина у пациентов младше 18 лет с аффективными расстройствами не установлены.
Ухудшение клинической картины и риск самоубийства, связанный с биполярным расстройством. У пациентов с биполярным расстройством может наблюдаться обострение депрессивных симптомов и/или появление суицидальных мыслей и поведения независимо от того, принимают ли они ЛС для лечения биполярного расстройства. Пациентов следует внимательно наблюдать на предмет ухудшения клинической картины (включая развитие новых симптомов) и суицидальности, особенно в начале курса лечения или при изменении дозы ЛС.
Кроме того, пациенты с суицидальным поведением или мыслями в анамнезе, пациенты, демонстрирующие значительную степень выраженности суицидальных мыслей до начала лечения, и молодые люди подвержены повышенному риску возникновения суицидальных мыслей или попыток самоубийства и должны находиться под тщательным наблюдением во время терапии.
Следует рассмотреть вопрос об изменении схемы лечения, включая возможное прекращение приема ЛС, у пациентов, у которых наблюдается клиническое ухудшение (включая развитие новых симптомов) и/или появление суицидальных мыслей/поведения, особенно если эти симптомы имеют тяжелую форму, обострение в начале их проявления или не являются симптомами, ранее наблюдавшимися у пациента.
Сообщалось о случаях передозировки ламотриджина, некоторые из которых приводили к летальному исходу. Для снижения риска передозировки ЛС, содержащие ламотриджин, следует назначать в минимальном объеме, соответствующем надлежащему ведению пациента.
Асептический менингит
Терапия ламотриджином повышает риск развития асептического менингита. В связи с возможностью серьезных исходов нелеченого менингита, вызванного другими причинами, пациенты должны пройти обследование для выявления причин менингита и получить соответствующее лечение.
В пострегистрационный период случаи развития асептического менингита были зарегистрированы у детей и взрослых пациентов, принимавших ламотриджин по различным показаниям. Симптомы при поступлении включали головную боль, лихорадку, тошноту, рвоту и ригидность затылочных мышц. В некоторых случаях также отмечались кожная сыпь, светобоязнь, миалгия, озноб, изменение сознания и сонливость. Сообщалось, что симптомы появлялись в течение от 1 дня до 1,5 мес после начала лечения. В большинстве случаев симптомы разрешались после прекращения приема ламотриджина. Возобновление приема приводило к быстрому возвращению симптомов (от 30 мин до 1 дня после возобновления лечения), которые часто имели более тяжелую форму. У некоторых пациентов, получавших терапию ламотриджином, асептический менингит развился на фоне основных заболеваний, таких как СКВ или другие аутоиммунные заболевания.
На момент клинической картины анализ спинномозговой жидкости в описанных случаях характеризовался легким или умеренным плеоцитозом, нормальным уровнем глюкозы и легким или умеренным повышением белка. Дифференциальный анализ количества лейкоцитов в спинномозговой жидкости в большинстве случаев показывал преобладание нейтрофилов, хотя примерно в 1/3 случаев отмечалось преобладание лимфоцитов. У некоторых пациентов также отмечалось появление признаков и симптомов поражения других органов (преимущественно печень и почки), что свидетельствовало о том, что в данных случаях наблюдавшийся асептический менингит был частью реакции гиперчувствительности.
Одновременное применение ламотриджина с пероральными контрацептивами
Было показано, что некоторые эстрогенсодержащие пероральные контрацептивы снижают концентрацию ламотриджина в сыворотке крови (см. «Взаимодействие»). Большинству пациентов, которые начинают или прекращают прием эстрогенсодержащих пероральных контрацептивов во время приема ламотриджина необходима коррекция дозы ламотриджина. При применении пероральных контрацептивов в период недельного перерыва без таблеток ожидается повышение концентрации ламотриджина в плазме крови, вплоть до 2-кратного к концу недели. Могут возникать нежелательные реакции, связанные с повышенной концентрацией ламотриджина, такие как головокружение, атаксия и диплопия.
Эпилептические (судорожные) припадки при отмене приема ламотриджина
Как и в случае приема других противоэпилептических ЛС, не следует резко отменять прием ламотриджина. У пациентов с эпилепсией существует вероятность увеличения частоты припадков. В клинических исследованиях у 2 пациентов с биполярным расстройством наблюдались эпилептические (судорожные) припадки вскоре после резкой отмены приема ламотриджина, однако наличие отягощающих факторов также могло способствовать возникновению судорожных припадков у этих пациентов. Если по соображениям безопасности более быстрая отмена не требуется, дозу ламотриджина следует снижать в течение не менее 2 нед (примерно на 50% в неделю).
Эпилептический статус
Достоверную оценку частоты возникновения эпилептического статуса, вызванного проводимой терапией, среди пациентов, принимавших ламотриджин, получить сложно, поскольку не все участники клинических исследований использовали одинаковые правила для выявления случаев. Как минимум у 7 из 2343 взрослых пациентов наблюдались эпизоды, которые можно однозначно охарактеризовать как эпилептический статус. Кроме того, было зарегистрировано несколько сообщений о различных эпизодах обострения эпилептических припадков (например, кластерные судороги, внезапные судорожные припадки).
Синдром внезапной смерть при эпилепсии
Во время дорегистрационных исследований ламотриджина было зарегистрировано 20 внезапных и необъяснимых случаев наступления смерти среди когорты из 4700 пациентов с эпилепсией (5747 пациенто-лет воздействия).
В некоторых из этих случаев наступления смерти, связанных с припадками, сам припадок не наблюдался, например, ночью. Частота встречаемости таких случаев составляет 0,0035 смертей на пациенто-год. Хотя этот показатель превышает ожидаемый для здоровой части населения, соответствующий возрасту и полу, он находится в пределах диапазона оценок частоты для синдрома внезапной смерти при эпилепсии у пациентов, не получающих ламотриджин (от 0,0005 в общей популяции пациентов с эпилепсией до 0,004 в популяции, изученной за последнее время в клинических исследованиях, сходной с таковой, принимающей участие в программе клинической разработки ламотриджина, и до 0,005 среди пациентов с рефрактерной эпилепсией). Следовательно, возможность считать данные показатели обнадеживающими или вызывающими беспокойство, зависит от сопоставимости ранее описанных популяций с когортой, получающей ламотриджин, и точности представленных оценок. Вероятно, наиболее обнадеживающим является сходство расчетных показателей для синдрома внезапной смерти при эпилепсии у пациентов, принимающих ламотриджин, и пациентов, принимающих другие противоэпилептические ЛС, имеющие различную химическую структуру, которые прошли клинические испытания в сходных популяциях. Следует подчеркнуть, что противоэпилептическое ЛС не должно быть химически родственно ламотриджину. Эти данные позволяют предположить, хотя и не доказывают, что высокие показатели для синдрома внезапной смерти при эпилепсии отражают популяционные показатели, а не эффект ЛС.
Ламотриджин в качестве дополнительной терапии к комбинированной схеме лечения, включающей вальпроат
Поскольку вальпроат снижает клиренс ламотриджина, доза ламотриджина в присутствии вальпроата составляет менее 1/2 дозы, необходимой при его отсутствии (см. «Взаимодействие»).
Связывание с меланином в тканях глаз и других меланинсодержащих тканях
Поскольку ламотриджин связывается с меланином, со временем он может накапливаться в тканях, богатых меланином. Это повышает вероятность того, что после длительного применения ламотриджин может вызвать токсичность в этих тканях. Хотя офтальмологическое тестирование проводилось в 1 контролируемом клиническом исследовании, его результатов недостаточно для исключения слабовыраженных эффектов или незначительных повреждений, возникающих после длительного воздействия. Более того, способность имеющихся тестов выявлять потенциально неблагоприятные последствия связывания ламотриджина с меланином, если таковые имеются, неизвестна.
Соответственно, несмотря на отсутствие конкретных рекомендаций по периодическому офтальмологическому мониторингу, при назначении ламотриджина необходимо учитывать возможность долговременных офтальмологических эффектов.
Лабораторные тесты
Ложноположительные результаты теста на наркотики. Сообщалось, что ламотриджин влияет на результаты анализа, используемого в некоторых экспресс-тестах мочи на наркотики, что может привести к ложноположительным результатам, особенно на фенциклидин (фенилциклогексилпиперидин). Для подтверждения положительного результата следует использовать более специфический аналитический метод.
Концентрация ламотриджина в плазме крови. Значимость мониторинга концентрации ламотриджина в плазме крови не установлена. Из-за возможного ФКВ ламотриджина и других ЛС, включая противоэпилептические, может быть показан мониторинг концентрации ламотриджина и сопутствующих ЛС в плазме крови, особенно при необходимости коррекции дозы. В большинстве случаев решение о мониторинге концентрации ламотриджина и других ЛС в плазме крови и необходимости коррекции дозы следует принимать на основании клинической оценки.
Особые группы пациентов
Дети. Ламотриджин показан в качестве дополнительной терапии у пациентов от 2 лет и старше при парциальных припадках, генерализованных припадках, при синдроме Леннокса-Гасто и первично-генерализованных тонико-клонических припадках.
Безопасность и эффективность ламотриджина в качестве дополнительной терапии при парциальных припадках не были продемонстрированы в небольшом рандомизированном двойном слепом плацебо-контролируемом исследовании отмены приема ламотриджина у самых маленьких пациентов (в возрасте от 1 до 24 мес). Применение ламотриджина было связано с повышенным риском инфекционных побочных реакций (ламотриджин 37%, плацебо 5%), таких как бронхиолит, бронхит, инфекция уха, инфекция глаз, наружный отит, фарингит, инфекция мочевыводящих путей и вирусная инфекция, и респираторных нежелательных реакций (ламотриджин 26%, плацебо 5%), таких как заложенность носа, кашель и апноэ.
Безопасность и эффективность применения ламотриджина у пациентов младше 18 лет с биполярным расстройством не установлены.
В исследовании на ювенильных животных, в котором ламотриджин (пероральные дозы 5, 15 или 30 мг/кг) вводили молодым крысам (постнатальные дни от 7 до 62), наблюдалось снижение жизнеспособности и роста при самой высокой дозе, а отдаленные поведенческие расстройства (снижение локомоторной активности, повышенная реактивность и дефицит обучения у взрослых животных) наблюдались при двух самых высоких дозах. Доза, при которой наблюдалось отсутствие эффекта неблагоприятного воздействия на нейроповеденческое развитие, была ниже, чем доза ламотриджина для человека 400 мг/сут в расчете на площадь поверхности тела.
Пожилой возраст. Клинические исследования ламотриджина для лечения эпилепсии и биполярного расстройства не включали достаточного количества пациентов в возрасте 65 лет и старше, чтобы определить, отличаются ли ответ на терапию или профиль безопасности у пациентов пожилого возраста от таковых у более молодых пациентов. Следует с осторожностью осуществлять подбор дозы для пациентов пожилого возраста, обычно начиная с нижней границы диапазона дозирования, что отражает бóльшую частоту снижения функции печени, почек или сердца, а также наличия сопутствующих заболеваний или другой лекарственной терапии.
Печеночная недостаточность. Опыт применения ламотриджина у пациентов с печеночной недостаточностью ограничен. На основании результатов клинического фармакологического исследования у 24 пациентов с нарушением функции печени легкой, средней и тяжелой степени тяжести можно дать следующие общие рекомендации. Для пациентов с нарушением функции печени легкой степени тяжести коррекция дозы не требуется. Начальные, эскалационные и поддерживающие дозы, как правило, должны быть снижены примерно на 25% у пациентов с нарушением функции печени средней и тяжелой степени без асцита и на 50% у пациентов с тяжелыми нарушениями функции печени с асцитом. Эскалационные и поддерживающие дозы следует корректировать в зависимости от клинического ответа.
Почечная недостаточность. Ламотриджин метаболизируется в основном путем конъюгации с глюкуроновой кислотой, при этом большинство метаболитов выделяется с мочой. В небольшом исследовании, в котором сравнивали однократную дозу ламотриджина у лиц с различной степенью нарушения функции почек и здоровых добровольцев, T1/2 ламотриджина из плазмы был примерно в 2 раза выше у лиц с ХПН.
Начальные дозы ламотриджина должны основываться на схемах приема противоэпилептических ЛС пациентами; сниженные поддерживающие дозы могут быть эффективны для пациентов со значительными нарушениями функции почек. Несколько пациентов с тяжелой почечной недостаточностью были обследованы во время длительного лечения ламотриджином. Поскольку опыт применения ламотриджина в этой популяции недостаточен, у таких пациентов ламотриджин следует применять с осторожностью.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.